- Tipps
- Technologie
- Häufig gestellte Fragen
- Tests
- mAh Kapazität
- Nennkapazität
- Vergleich
- everActive
- Batterien vs. wiederaufladbare Batterien
- Akkumulierte Energie
- Haltbarkeit von wiederaufladbaren Batterien
- Effizienz von wiederaufladbaren Batterien
- Batteriespannung
- LR03 AAA
- LR6 AA
- eneloop
- AG13 LR1154 LR44
- CR 2032
- Delta V
- Ladezyklen
- Innenwiderstand
- Ladezustand
- Memory-Effekt
- Akkreditierte Prüfung
- SR44 357
- Hörbatterien 675
- SR626 377
- Uhren-Batterien
- Polarität
- Mah
- Passivierung
- ls 14250
- LS 14500
Wie funktioniert der Akku?
2019-06-19
Wenn wir uns die Batterie ansehen, können wir sehen, dass sie zwei Pole hat - einen positiven, mit "+" gekennzeichnet, den anderen negativen - mit "-". Bei typischen zylindrischen Batterien wie R6/AA oder R14/C (die z. B. zur Stromversorgung von Taschenlampen oder Spielzeug verwendet werden) sind die Pole die Enden der Batterie. Bei Autobatterien sind die Pole schwere Bleiklemmen.
Elektronen sammeln sich am Minuspol der Batterie. Wenn wir den Minus- und den Pluspol mit einem Draht verbinden, bewegen sich die Elektronen so schnell wie möglich vom Minuspol zum Pluspol - die Batterie wird sehr schnell leer (außerdem raten wir aufgrund der damit verbundenen Gefahren von dieser Art von Experimenten ab - schließen Sie die Batterie niemals auf diese Weise "für kurze Zeit" kurz!). Unter normalen Bedingungen verbinden wir eine Last mit einem Kabel mit der Batterie - einer Glühbirne, einem Motor oder einer elektronischen Schaltung, wie z. B. einem Radio.
Im Inneren der Batterie findet eine Reaktion statt, bei der freie Elektronen entstehen. Die Geschwindigkeit, mit der durch diese Reaktion Elektronen freigesetzt werden (Innenwiderstand - Widerstand - der Batterie), begrenzt offensichtlich die Anzahl der Elektronen, die zwischen den Polen fließen können. Elektronen müssen von der Batterie durch den Draht und die Last, vom Minuspol zum Pluspol fließen, damit eine chemische Reaktion stattfinden kann, die noch mehr von ihnen freisetzt. Aus diesem Grund können wir die Batterie z.B. ein Jahr unbenutzt im Regal stehen lassen, um sie dann problemlos weiter zu verwenden – solange die Elektronen nicht vom Minus- in den Pluspol fließen, findet die chemische Reaktion nicht statt. In dem Moment, in dem die Pole verbunden sind, beginnt die Reaktion.
Chemische Reaktionen in Batterien
Eine der einfachsten Batterien ist die Zink-Kohle-Batterie. Wenn wir uns die Reaktionen ansehen, die in ihm ablaufen, können wir das allgemeine Funktionsprinzip aller Batterien leichter verstehen. Stellen Sie sich vor, wir haben ein Glas Schwefelsäure (H2SO4). Wenn Sie einen Zinkstab hineinlegen, beginnt die ätzende Säure sofort, ihn aufzulösen. Wir werden sehen, wie sich Wasserstoffblasen auf der Oberfläche des Zinks ansammeln, und sowohl der Stab als auch die Säure beginnen sich zu erhitzen.Folgendes passiert:
- Säuremoleküle zerfallen in drei Ionen: zwei H+-Ionen und ein SO4-Ion
- Zinkatome auf der Oberfläche des Stabes verlieren zwei Elektronen (2e-) und werden zu Zn++-Ionen
- Zn++-Ionen verbinden sich mit SO4---Ionen zu ZnSO4, das sich in Säure auflöst
- Elektronen aus Zinkatomen verbinden sich mit H+-Ionen und bilden H2-Moleküle (Wasserstoffgas)
- Die Elektronen werden sich entlang des Drahtes bewegen und sich mit dem Wasserstoff auf dem Kohlenstoffstab verbinden, aus dem sich nun auch Wasserstoffblasen zu entwickeln beginnen
- Die Wärmefreisetzung wird erheblich reduziert; Mit dem Strom, der jetzt durch den Draht fließt, könnten wir zum Beispiel eine Glühbirne mit Strom versorgen - und die resultierende Spannung und den Strom messen, die durch den Draht fließen - ein Teil der Wärmeenergie wurde in die Bewegung von Elektronen umgewandelt.
Die Batterien, die wir kennen, funktionieren nach dem gleichen Prinzip. Sie unterscheiden sich in der Art der verwendeten Metalle und Elektrolyte, aber sie funktionieren alle dank des gleichen Phänomens - Elektronen, die von einem Pol zum anderen fließen. Abhängig von den verwendeten Komponenten ändert sich auch die charakteristische Spannung einer solchen Batterie. Folgen wir dem Beispiel einer typischen Blei-Autobatterie:
- Die Batterie enthält eine Platte aus Blei und eine aus Bleidioxid, die beide in einen Elektrolyten aus hochkonzentrierter Schwefelsäure getaucht sind
- Blei verbindet sich mit SO4 zu PbSO4 und einem freien Elektron
- Bleidioxid, Wasserstoffionen und SO4-Ionen sowie Elektronen aus der Bleiplatte bilden PbSO4 und Wasser auf der Platte aus Bleidioxid Im Laufe der Zeit werden die beiden Platten mit PbSO4 beschichtet und das Wasser vermischt sich mit der Säure; Die charakteristische Spannung beträgt etwa 2 V - wenn wir also 6 Zellen in Reihe schalten, erhalten wir eine Batterie von Zellen mit einer Spannung von 12 V
- Zink-Kohle-Batterien - so beliebt, dass sie manchmal als "gewöhnlich" bezeichnet werden; sind die am häufigsten verwendeten Batterien, in Größen wie R6/AA, R14/C, R20/D; die Elektroden bestehen aus Zink und
- Kohlenstoff, zwischen dem eine saure Paste eingeklemmt ist, die als Elektrolyt dient
- Batterien A
Zell-/Batterie-Verklebung
In den vorherigen Überlegungen haben wir die Wörter "Batterie" und "Zelle" synonym verwendet. Dies entspricht der Tendenz, die in der Alltagssprache vorherrscht. Aus technischer Sicht haben die Wörter "Batterie" und "Zelle" jedoch recht unterschiedliche Bedeutungen. "Zelle" meint also eine einzelne Energiequelle, wie z.B. das eingangs beschriebene Säuregefäß und zwei Stäbe, die mit einem Draht (oder z.B. einem R6/AA-"Finger") verbunden sind. Eine "Batterie" ist ein Satz verbundener Zellen (z. B. eine 3R12-Batterie, bestehend aus drei Zellen in einem Gehäuse, die in Reihe geschaltet sind). In diesem Sinne werden wir diese beiden Begriffe im folgenden Teil dieses Textes verwenden.In den meisten Geräten neigen wir dazu, keine einzelne Zelle zu verwenden. Stattdessen schalten wir mehrere davon in Reihe – entweder in Reihe, für höhere Spannungen, oder parallel, für höhere Ströme. Bei der Reihenschaltung erhalten wir die Summe der Spannungen der angeschlossenen Zellen; in Parallelschaltung - die Summe der Ströme, die von den Komponentenzellen erhalten werden.
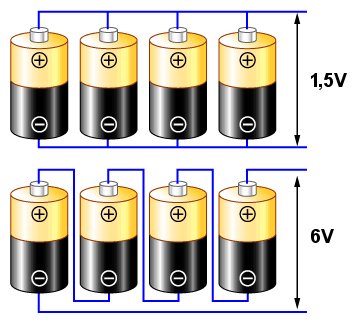
Die Verbindung wie im oberen Diagramm wird als parallel bezeichnet. Wenn wir davon ausgehen, dass jede Zelle eine charakteristische Spannung von 1,5 V hat (wie eine typische einzelne Zink-Kohle- oder Alkalizelle), dann beträgt die an den Endklemmen (durch Pfeile gekennzeichnete) erhaltene Spannung immer noch 1,5 V, aber der erhaltene Strom ist viermal höher als der einer einzelnen Zelle.
Die Verbindung wie im unteren Diagramm wird als seriell bezeichnet. In diesem Fall addieren sich die Spannungen der einzelnen Zellen, so dass zwischen den Klemmen eine Spannung von 6V entsteht.
Beim Kauf eines Akkus oder einer Zelle kann man in der Regel auf der Verpackung ablesen, wie hoch die Spannung ist – manchmal auch die Kapazität. Zum Beispiel haben typische wiederaufladbare Batterien, die in Digitalkameras verwendet werden, eine Spannung von 1,2 V und eine Kapazität von 2000 mAh. Eine Kapazität von 2000 mAh (mAh ist eine Abkürzung für Milliampere-Stunde) bedeutet, dass eine solche Batterie theoretisch in der Lage ist, einen Strom von 2000 mA (2000 Milliampere, d.h. 2 Ampere) für eine Stunde, einen Strom von 1 A für zwei Stunden, einen Strom von 100 mA für 20 Stunden usw. zu liefern. Zellen verhalten sich jedoch in der Regel nicht so linear. Erstens hat jede Batterie einen maximalen Strom, den sie liefern kann. Und so wird eine 500-mAh-Batterie nicht in der Lage sein, eine Sekunde lang 30 A Strom zu liefern, da es für die chemischen Reaktionen, die in der Batterie ablaufen, keine Möglichkeit gibt, so viele Elektronen in so kurzer Zeit bereitzustellen. Zweitens heizen sich die Zellen bei hohen Strömen in der Regel stark auf, wodurch viel Energie verschwendet wird. Drittens halten viele der in Batterien verwendeten chemischen Systeme kürzer (oder länger!) bei sehr geringem Stromverbrauch. Nichtsdestotrotz gibt die in Amperestunden gemessene Kapazität eine gute Vorstellung davon, wie lange eine bestimmte Zelle bei einem bestimmten Stromverbrauch unter typischen Betriebsbedingungen hält.
Urheberrecht © Baltrade
Kommentar hinzufügen