Catégories
- Conseils
- Technologie
- Foire aux questions
- Tests
- Capacité mAh
- Capacité nominale
- comparaison
- everActive
- Piles vs piles rechargeables
- Énergie accumulée
- Durabilité des batteries rechargeables
- Efficacité des batteries rechargeables
- tension de la batterie
- LR03 AAA
- LR6 AA
- eneloop
- AG13 LR1154 LR44
- CR 2032
- Delta V
- Charge Cycles
- résistance interne
- Niveau de charge
- effet mémoire
- test accrédité
- SR44 357
- Piles auditives 675
- SR626 377
- Piles de montres
- Polarité
- Mah
- Passivation
- LS 14250
- LS 14500
Comment fonctionne la batterie ?
2019-06-19
En regardant la batterie, nous pouvons voir qu’elle a deux pôles - l’un positif, marqué « + », l’autre négatif - marqué « -« . Dans le cas des piles cylindriques typiques, telles que R6/AA ou R14/C (utilisées, par exemple, pour alimenter des lampes de poche ou des jouets), les bornes sont les extrémités de la batterie. Dans les batteries de voiture, les pôles sont de lourdes bornes en plomb.
Les électrons s’accumulent sur le pôle négatif de la batterie. Si nous connectons les bornes négative et positive avec un fil, les électrons se déplaceront le plus rapidement possible de la borne négative à la borne positive - la batterie s’épuisera très rapidement (de plus, nous déconseillons ce type d’expériences en raison des dangers qui y sont associés - ne court-circuitez jamais la batterie de cette manière « pendant une courte période » !). Dans des conditions normales, nous connectons une charge à la batterie à l’aide d’un câble - une ampoule, un moteur ou un circuit électronique, tel qu’une radio.
À l’intérieur de la batterie, une réaction a lieu qui produit des électrons libres. La vitesse à laquelle les électrons sont libérés à la suite de cette réaction (résistance interne - résistance - de la batterie) limite évidemment le nombre d’électrons qui peuvent circuler entre les pôles. Les électrons doivent circuler de la batterie à travers le fil et la charge, de la borne négative à la borne positive, pour qu’une réaction chimique se produise qui en libérera encore plus. Pour cette raison, nous pouvons laisser la batterie inutilisée sur l’étagère pendant un an, par exemple, puis continuer à l’utiliser sans aucun problème - tant que les électrons ne circulent pas de la borne négative à la borne positive, la réaction chimique n’a pas lieu. Au moment où les pôles sont connectés, la réaction commence.
Réactions chimiques dans les batteries
L’une des batteries les plus simples est la batterie zinc-carbone. En regardant les réactions qui se déroulent à l’intérieur, nous pouvons plus facilement comprendre le principe général de fonctionnement de toutes les batteries. Imaginons que nous ayons un pot d’acide sulfurique (H2SO4). Si vous y placez une tige de zinc, l’acide corrosif commencera immédiatement à le dissoudre. Nous verrons des bulles d’hydrogène s’accumuler à la surface du zinc, et la tige et l’acide commenceront à se réchauffer.Voici ce qui se passe :
- les molécules d’acide se désintègrent en trois ions : deux ions H+ et un ion SO4
- les atomes de zinc à la surface de la tige perdent deux électrons (2e-) et deviennent des ions Zn++
- Les ions Zn++ se combinent avec les ions SO4 pour former le ZnSO4, qui se dissout dans l’acide
- les électrons des atomes de zinc se combinent avec les ions H+ et forment des molécules H2 (hydrogène gazeux)
- Les électrons commenceront à se déplacer le long du fil et à se combiner avec l’hydrogène sur la tige de carbone, à partir de laquelle des bulles d’hydrogène commenceront également à évoluer
- le dégagement de chaleur sera considérablement réduit ; En utilisant l’électricité qui circule maintenant dans le fil, nous pourrions, par exemple, alimenter une ampoule électrique - et mesurer la tension et le courant résultants circulant dans le fil - une partie de l’énergie thermique a été convertie en mouvement d’électrons.
Les batteries que nous connaissons fonctionnent sur le même principe. Ils diffèrent par les types de métaux et d’électrolytes utilisés, mais ils fonctionnent tous grâce au même phénomène : les électrons circulent d’un pôle à l’autre. En fonction des composants utilisés, la tension caractéristique d’une telle batterie change également. Suivons l’exemple d’une batterie au plomb typique d’une voiture :
- La batterie contient une plaque en plomb et une autre en dioxyde de plomb, toutes deux immergées dans un électrolyte d’acide sulfurique hautement concentré
- le plomb se combine avec le SO4 pour former du PbSO4 et un électron libre
- le dioxyde de plomb, les ions hydrogène et les ions SO4, ainsi que les électrons de la plaque de plomb, forment le PbSO4 et l’eau sur la plaque à partir du dioxyde de plomb au fil du temps, les deux plaques se recouvrent de PbSO4 et l’eau se mélange à l’acide ; la tension caractéristique est d’environ 2V - donc, en connectant 6 cellules en série, nous obtenons une batterie de cellules avec une tension de 12V
- piles zinc-carbone - si populaires qu’elles sont parfois appelées « ordinaires » ; sont les piles les plus couramment utilisées, dans des tailles telles que R6/AA, R14/C, R20/D ; les électrodes sont en zinc et
- carbone, avec une pâte acide prise en sandwich entre eux, servant d’électrolyte
- Piles A
Liaison cellule/batterie
Dans les considérations précédentes, nous avons utilisé les mots « batterie » et « pile » de manière interchangeable. Cela correspond à la tendance qui prévaut dans le langage courant. Cependant, d’un point de vue technique, les mots « batterie » et « pile » ont des significations très différentes. Ainsi, « pile » signifie une seule source d’énergie, par exemple le pot d’acide décrit au début et deux tiges reliées par un fil (ou, par exemple, un « doigt » R6/AA). Une « batterie » est un ensemble de cellules connectées (comme une batterie 3R12, composée de trois cellules dans un seul boîtier, connectées en série). C’est en ce sens que nous utiliserons ces deux termes dans la partie suivante de ce texte.Dans la plupart des appareils, nous avons tendance à ne pas utiliser une seule cellule. Au lieu de cela, nous en connectons plusieurs - soit en série, pour une tension plus élevée, soit en parallèle, pour des courants plus élevés. Dans la connexion en série, nous obtenons la somme des tensions des cellules connectées ; En connexion parallèle - la somme des courants obtenus à partir des cellules composantes.
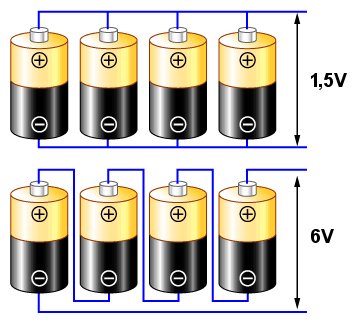
La connexion, comme dans le schéma supérieur, est appelée parallèle. Si nous supposons que chaque pile a une tension caractéristique de 1,5 V (comme une pile zinc-carbone ou alcaline typique), alors la tension obtenue aux bornes d’extrémité (indiquées par des flèches) sera toujours de 1,5 V, mais le courant obtenu sera quatre fois supérieur à celui obtenu d’une seule pile.
La connexion comme dans le schéma du bas est appelée série. Dans ce cas, les tensions des cellules individuelles s’additionnent, ce qui donne une tension de 6V entre les bornes.
Lors de l’achat d’une batterie ou d’une cellule, vous pouvez généralement lire sur l’emballage quelle est sa tension - parfois aussi sa capacité. Par exemple, les batteries rechargeables typiques utilisées dans les appareils photo numériques ont une tension de 1,2 V et une capacité de 2000 mAh. Une capacité de 2000mAh (mAh est l’abréviation de milliampères-heure) signifie que, théoriquement, une telle batterie est capable de fournir un courant de 2000mA (2000 milliampères, soit 2 ampères) pendant une heure, un courant de 1A pendant deux heures, un courant de 100mA pendant 20 heures, etc. Cependant, les cellules ne se comportent généralement pas de manière aussi linéaire. Tout d’abord, chaque batterie dispose d’un courant maximum qu’elle est capable de délivrer. Ainsi, une batterie de 500 mAh ne sera pas en mesure de fournir 30 A de courant pendant une seconde, car il n’y a aucun moyen pour les réactions chimiques qui ont lieu à l’intérieur de la batterie de fournir autant d’électrons en si peu de temps. Deuxièmement, à des courants élevés, les cellules chauffent généralement beaucoup, ce qui gaspille beaucoup d’énergie. Troisièmement, de nombreux systèmes chimiques utilisés dans les batteries durent moins longtemps (ou plus longtemps !) avec une très faible consommation d’énergie. Néanmoins, la capacité mesurée en ampères-heures donne une bonne idée de la durée de vie d’une cellule donnée à une certaine consommation de courant, dans des conditions de fonctionnement typiques.
Droits d’auteur © Baltrade
Ajouter un commentaire